Articles
- Page Path
- HOME > J Korean Soc Clin Toxicol > Volume 21(2); 2023 > Article
-
Original Article
약물농도를 알 수 없는 환경에서 acetaminophen 급성 중독환자의 안전한 N-acetylcysteine 치료 종료를 위한 혈중약물 검출 예측 -
김다해1,2
 , 차경만1,2
, 차경만1,2 , 소병학1,2
, 소병학1,2
- Predicting serum acetaminophen concentrations in acute poisoning for safe termination of N-acetylcysteine in a resource-limited environment
-
Dahae Kim, B.S.1,2
 , Kyungman Cha, M.D.1,2
, Kyungman Cha, M.D.1,2 , Byung Hak So, M.D.1,2
, Byung Hak So, M.D.1,2
-
Journal of The Korean Society of Clinical Toxicology 2023;21(2):128-134.
DOI: https://doi.org/10.22537/jksct.2023.00013
Published online: December 29, 2023
- 644 Views
- 13 Download
1가톨릭대학교 성빈센트병원 응급의학과
2가톨릭대학교 의과대학 응급의학교실
1Department of Emergency Medicine, St. Vincent’s Hospital, Suwon, Korea
2Department of Emergency Medicine, College of Medicine, The Catholic University of Korea, Seoul, Korea
- Corresponding author: Kyungman Cha Department of Emergency Medicine, St. Vincent's Hospital, 93 Jungbu-daero, Paldal-gu, Suwon 16247, Korea Tel: +82-31-249-7363 Fax: +82-31-253-4126 E-mail: drchaa@catholic.ac.kr
• Received: September 26, 2023 • Revised: October 10, 2023 • Accepted: October 18, 2023
Copyright © Korean Society of Clinical Toxicology
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
-
Purpose
- The Prescott nomogram has been utilized to forecast hepatotoxicity from acute acetaminophen poisoning. In developing countries, emergency medical centers lack the resources to report acetaminophen concentrations; thus, the commencement and cessation of treatment are based on the reported dose. This study investigated risk factors that can predict acetaminophen detection after 15 hours for safe treatment termination.
-
Methods
- Data were collected from an urban emergency medical center from 2010 to 2020. The study included patients ≥14 years of age with acute acetaminophen poisoning within 15 hours. The correlation between risk factors and detection of acetaminophen 15 hours after ingestion was evaluated using logistic regression, and the area under the curve (AUC) was calculated.
-
Results
- In total, 181 patients were included in the primary analysis; the median dose was 150.9 mg/kg and 35 patients (19.3%) had acetaminophen detected 15 hours after ingestion. The dose per weight and the time to visit were significant predictors for acetaminophen detection after 15 hours (odds ratio, 1.020 and 1.030, respectively). The AUCs were 0.628 for a 135 mg/kg cut-off value and 0.658 for a cut-off 450 minutes, and that of the combined model was 0.714 (sensitivity: 45.7%, specificity: 91.8%).
-
Conclusion
- Where acetaminophen concentrations are not reported during treatment following the UK guidelines, it is safe to start N-acetylcysteine immediately for patients who are ≥14 years old, visit within 15 hours after acute poisoning, and report having ingested ≥135 mg/kg. Additional N-acetylcysteine doses should be considered for patients visiting after 8 hours.
- 지난 수십 년간 acetaminophen (N-acetyl-paraminophenol, APAP) 급성 중독환자의 간 독성 발생위험 예측, N-acetylcysteine (NAC) 길항제 치료 필요성과 치료 종료 결정을 위하여 Prescott nomogram을 이용해 왔다1,2). 현재 영국을 비롯한 몇몇 국가에서는 100-치료선(음독 4시간 후 100 μg/mL, 12시간 후 25 μg/mL)을, 미국을 비롯한 많은 국가에서는 150-치료선(음독 4시간 후 150 μg/mL, 12시간 후 37.5 μg/mL)을 치료기준으로 사용하고 있다2-6).
- 그러나 일부 개발도상국의 응급의료센터는 APAP 혈중 약물농도를 환자 치료 중 적시에 보고하는 데 필요한 실험실 시설을 갖추고 있지 않기 때문에, NAC 투여 시작과 종료 결정을 거의 전적으로 환자와 보호자로부터 얻은 APAP 음독 추정용량, 일반 혈액검사 결과와 환자의 임상증상에 의존하고 있다7-9).
- 본 연구의 목적은 APAP 혈중농도를 치료 중 보고받을 수 없는 환경에서, 영국 지침에 따라 APAP 급성 중독환자를 치료할 때, 안전한 NAC 길항제 치료 종료를 위해 National Health Service 지침의 NAC 추가용량 치료기준 중 하나인10,11), 음독 15시간 후 APAP 혈중농도 검출을 예측할 수 있는 임상 위험인자를 조사하는 것이다.
서론
- 2010년 1월 1일부터 2020년 12월 31일까지 총 132개월간, 대한민국 경기도 수원시에 위치한 매년 6만 명 이상의 환자가 내원하는 대학병원 응급의료센터의 독극물 음독 환자 데이터베이스에서 후향적으로 자료를 추출하였다. 음독 환자 데이터베이스는 환자가 내원했을 때 근무 중인 당직 전문의가 디지털 방식으로 미리 정해진 양식에 따라 기록한 자료이다. 본 연구는 가톨릭대학교 수원 성빈센트병원 임상윤리위원회의 승인을 얻은 후 진행되었고(XC23RIDI0008), 후향적 연구임을 인정받아, 환자 동의서는 면제받았다.
- 1. 연구 모집단
- 최대 치료용량인 75 mg/kg/day 이상의 APAP 음독 후 15시간이 경과되기 전 내원한 14세 이상의 급성 중독환자를 연구에 포함시켰고, 만성 간질환 환자, coumadin 복용 중인 환자, 1시간 이상의 시간 동안 여러 번 음독한 중복 음독 환자, 서방정을 음독한 환자, 응급의료센터에서 활성탄 치료를 받은 환자, 음독용량, 체중, APAP 혈중농도 자료가 누락되어 있는 환자는 연구에서 제외하였다.
- 2. 자료수집
- 환자의 나이, 성별, 체중, 환자 혹은 보호자, 구급대원이 알려준 총 음독용량과 음독시각, 응급의료센터에 내원할 때까지 경과한 시간, 음독의 고의성, APAP의 단일제제 혹은 복합제제의 여부, 복합제 내 혼합약물 성분, 서방정 유무, 동반 음독약물의 성분, 만성 음주 여부, anorexia nervosa와 같은 식이장애 여부, NAC 길항제 치료 여부, 치료 시작 및 종료 시각, 혈액화학검사 결과, 음독 후 시간경과에 따른 APAP 혈중농도, 임상경과를 수집하였다.
- 환자, 보호자 혹은 구급대원이 알려준 여러 음독용량 중, 가장 높은 용량을 음독용량으로 추정했고, 내원까지 경과시간 역시 가장 긴 시간을 경과시간으로 판단했다. 복합제 내 혼합 성분과 동반 음독약물 성분은 환자, 보호자 혹은 구급대원이 진술했거나, 응급의료센터로 가져온 남아있는 약물, 처방전 혹은 처방 병원에 연락하여 알아낸 모든 약물을 기록하였다. 만성 음주력은 일주일간 14 standard alcohol doses를 초과하는 음주로 정의하였다. 급성 간 손상(acute liver injury)은 치료기간 중 alanine aminotransferase (ALT) 50% 이상의 상승으로 정의하였고, 급성 간 독성(acute hepatotoxicity)은 ALT가 1,000 IU/L 초과하는 상승으로 정의하였다3). APAP 혈중농도 검사시각은 결과 보고지에 기록된 시각을 분단위로 기록하였고, 음독 후 4시간(240분) 이전에 시행된 검사결과는 인정하지 않고, 그 다음 검사한 검사시각과 혈중농도를 최초 검사결과로 기록하였다.
- 연구기간에 NAC 길항제 사용기준은 24시간 내 총 음독용량 10 g 혹은 체중 1 kg당 200 mg 이상의 음독용량, 1시간 이상의 시간 동안 중복음독, 그리고 불명확한 음독 시간이었다. NAC 길항제 치료는 NAC 150 mg/kg을 15분간, 45분 후 50 mg/kg을 4시간 동안, 그리고 100 mg/kg을 16시간 동안 정주하는 21시간 정주 프로토콜을 따랐다. NAC 정주치료 종료 1시간 전, 의식장애, 황달, 우상복부의 동통이 있거나, 혈액화학검사 결과 ALT, international normalized ratio (INR) 혹은 creatinine이 치료 시작 전보다 50% 이상 상승하면, NAC 100 mg/kg 16시간 정주치료를 추가로 시행했고, 임상증상이 사라지고, aspartate aminotransferase ≤1,000 IU/L, INR ≤1.3 그리고 creatinine ≤1.2 될 때까지 추가 치료를 계속했다.
- APAP 혈중농도 측정을 위한 혈액샘플 채취는 음독 후 4시간 경과마다, NAC 길항제 치료 종료 1시간 전 채취를 포함하여, 급성 간 손상이 발생하는 환자들의 치료계획을 위해 최소 3회 시행되었다. 본 연구가 시행된 응급의료센터는 APAP 혈중농도를 적시에 보고할 수 있는 임상병리시설이 갖추어져 있지 않아, 외부 전문 임상검사기관에 검체 분석을 의뢰하여 결과를 추후 확정하였다(서울 의과학연구소; Seoul Clinical Laboratories, Yongin, Korea). 위 검사기관의 APAP 희석 후 검출 최소농도는 0.7 μg/mL이고, 진단검사시스템은 Cobas 8000 (Roche Diagnostics, Mannheim, Germany)이었다.
- 3. 통계분석
- Kolmogorov-Smirnov법을 이용하여 변수들의 정규성을 검사하였다. 연속형 변수는 정규분포를 따르는 경우 평균값을, 그렇지 않은 경우 중앙값을 구하였고, 범주형 변수는 비율을 구하였다. χ2 및 Mann-Whitney U test을 사용하여, 음독 15시간 이후 APAP 혈중농도가 검출되는 그룹과 검출되지 않는 그룹 간 변수들의 비율과 분포를 비교했다. NAC 길항제 치료를 예측할 수 있는 것으로 알려져 있는 위험인자들과 음독 15시간 이후 APAP 혈중농도 검출 여부와 상관관계를 단순 및 다중 로지스틱 회귀분석을 사용하여 분석하였고, odds ratio (OR) 및 95% confidence interval (CI)을 계산하였다. 음독 15시간 이후 APAP 혈중농도 검출 예측을 위한 위험인자들의 receiver operating characteristic 곡선을 그려, the area under the curve (AUC)를 계산하였다.
대상과 방법
- 1. 연구 모집단
- 연구기간에 총 502명의 APAP 급성 중독환자가 내원하였고, 그 중 만 14세 미만 21명과 75 mg/kg 이하의 용량을 음독 후 내원한 환자 26명을 제외하였다(14세 미만이고 75 mg/kg 이하 용량을 음독한 환자 30명). 의무기록상 음독용량과 체중정보가 남아있지 않은 환자 각 24명과 84명(음독용량과 체중정보 모두 누락된 환자 8명), APAP 혈중농도 자료가 누락된 환자 38명을 제외하였다. 음독 후 15시간 초과하여 내원한 환자 46명, 1시간 이상의 시간 동안 여러 번 음독한 중복 중독환자 12명, 서방정을 음독한 환자 86명, 만성 간질환 환자 2명, 응급의료센터에 활성탄 치료를 받은 환자 39명을 제외한(서방정을 음독하고 활성탄 치료를 받은 환자 19명), 총 181명의 환자를 연구에 포함시켰다(Fig. 1).
- 29명의 환자가 남성이었고(16.0%), 연령 중앙값은 22세(interquartile range [IQR], 17–33세), 171명의 환자가 의도적으로 음독하였다(94.5%). 환자들의 단위체중당 음독용량의 중앙값은 150.9 mg/kg (IQR, 98.4–236.0 mg/kg)이었다(Table 1). 112명의 환자가 복합제제를 포함하여 다른 성분의 약물을 동시에 음독하였고(61.9%), nonsteroidal anti-inflammatory drug 39예(21.5%), caffeine 26예(14.4%), decongestants 19예(10.5%), benzodiazepine 15예(8.3%) 순이었다. 이 중 27명의 환자가 pheniramine, chlorpheniramine, methylphenidate, cetirizine, codeine, dihydrocodeine, levodopa, carbidopa 등 위장관 운동을 저하시키는 약물을(14.9%), 25명의 환자가 scopolamine, diphenhydramine, levocetirizine, dextromethorphan 같은 간 효소 유도약물을 동반 음독하였다(13.9%).
- 80명의 환자가 총 10 g 이상 혹은 체중 1 kg당 200 mg 이상의 APAP를 음독하였고(44.2%), 이들 모두 NAC 길항제 치료를 받았다. 61명의 환자가 첫 번째 APAP 혈중농도 검사에서 100-치료선 이상의 독성 농도를 보였고(33.7%), 첫 번째 검사까지 소요시간의 중앙값은 355분이었다(IQR, 267–508분). 총 4명의 환자가 급성 간 독성을 보여, 기존의 연구들의 결과들과 큰 차이는 없었고2,4,6,9), 모두 NAC 정주치료만 받고 후유증 없이 퇴원하였다. 100-치료선 위의 독성 농도 예측을 위한 단위체중당 음독용량의 AUC는 0.827 (95% CI, 0.764–0.879; p<0.001), 150 mg/kg 절단값의 민감도와 특이도는 88.5% (77.8%–95.3%) 및 67.5% (58.3%–75.8%)였다(Fig. 2).
- 총 7명의 환자가 첫 번째 APAP 혈중농도 검사에서 비독성 농도를, 두 번째 검사에서 독성 농도를 보였다(line-crossers). 이 중 3명의 환자가 diphenhydramine을 동반 음독한 것 외에 line-cross를 일으킬 수 있는 위험인자가 없었고, 이 중 750 mg/kg 음독 후 6시간 경과하여 내원한 17세 여성 환자가 급성 간 독성을 보였으나(peak ALT 6,825 IU/L, peak INR 3.87), 8일간 4번의 NAC 100 mg/kg 추가 정주치료 후 후유증 없이 퇴원하였다.
- 총 35명의 환자가 음독 후 15시간 경과 후 APAP 혈중농도가 검출되었다(19.3%). 이 중 4명의 환자는 첫 번째 APAP 혈중농도 검사가 음독 15시간 이후에 시행되었고, 총 4명의 환자가 급성 간 독성을 보였다. 4명 중 한 명은 위에서 언급한 line-cross를 보인 환자이고, 다른 세 명은 각각 333 mg/kg을 음독하고 13시간 후 내원(peak ALT 6,819 IU/L, peak INR 1.88), 500 mg/kg을 음독하고 1시간 후 내원(peak ALT 6,631 IU/L, peak INR 2.95), 555 mg/kg을 음독하고 9시간 후 내원한 환자였다(peak ALT 4,550 IU/L, peak INR 2.16). 세 환자 각각 3번, 4번, 2번의 NAC 100 mg/kg 추가 정주치료 후 후유증 없이 퇴원하였다.
- 2. NAC 길항제 치료 예측의 위험인자와 음독 15시간 후 APAP 혈중농도 검출 간의 상관관계
- 다중 로지스틱 회귀분석을 통하여, NAC 길항제 치료를 예측할 수 있는 것으로 알려져 있는 위험인자들이 음독 15시간 후 APAP 혈중농도 검출을 예측할 수 있는지 알아보았고, 단위체중당 음독용량 그리고, 음독 후 응급의료센터 내원까지 소요된 시간만이 음독 15시간 후 혈중농도 검출을 예측할 수 있었다(OR, 1.020; 95% CI, 1.001–1.042; p=0.042; OR, 1.030; 95% CI, 1.013–1.048; p<0.001) (Table 2).
- 음독 15시간 후 APAP 혈중농도 검출 예측을 위한 단위체중당 음독용량의 AUC는 0.628 (95% CI, 0.554–0.699; p=0.014), 135 mg/kg 절단값의 민감도와 특이도는 77.1% (59.9%–89.6%) 및 48.0% (39.6%–56.4%)였고, 음독 후 내원까지 소요시간의 AUC는 0.658 (95% CI, 0.583–0.726; p=0.004), 450분 절단값의 민감도와 특이도는 40.0% (23.9%–57.9%) 및 85.6% (78.9%–90.9%)였다. 위 두 변수를 결합시킨 예측모델의 AUC 값을 계산하였고, 그 값은 0.714 (95% CI, 0.642–0.778; p<0.001), 절단값의 민감도와 특이도는 45.7% (28.8%–63.4%) 및 91.8% (86.1%–95.7%)였다. 결합 예측모델, 단위체중당 음독용량, 음독 후 내원까지 소요시간의 AUC 값을 비교하기 위해 비모수적 방법으로 이원 비교하였고(pair-wise comparison), 결합모델과 음독 후 내원까지 소요시간만이 통계적으로 유의한 차이를 보였다(p=0.046) (Fig. 3, Table 3).
결과
- 의무기록에 음독용량과 체중정보가 남아있지 않은 환자 각 24명과 84명이 본 연구에 포함되지 않았다. 음독용량이 누락되어 있는 환자들 모두 NAC 길항제 치료를 받지 않은 것으로 보아, 매우 적은 용량을 음독한 것으로 판단했던 것으로 보인다. 모집단 체중의 중앙값(57.0 kg)을 사용하여 계산하면, 74명의 환자가 ≤75 mg/kg 용량의 APAP를 음독했을 것이라고 판단된다. 그리고 APAP 혈중농도 자료가 누락된 환자 38명 중 29명의 환자가 ≤75 mg/kg 용량의 APAP를 음독하였다. 따라서 상대적으로 작은 용량을 음독한 환자들이 더 많이 분석에서 제외되어, 첫 번째 APAP 혈중농도 검사에서 100-치료선 이상의 독성 농도를 보인 빈도와 음독 15시간 후 APAP 혈중농도 검출빈도가 과장되었을 가능성이 있다.
- 총 112명의 환자가 다른 성분의 약물을 동시에 음독했고, 38명의 환자가 위장관 운동을 저하시키거나, 간 효소를 유도하는 약물을 같이 음독했다. Line-cross phenomenon을 보인 7명의 환자 중 3명이 diphenhydramine을 같이 음독하기도 했다. Acetaminophen 흡수와 대사에 영향을 미치는 약물이 그 효과를 나타내려면 일정 용량 이상 음독해야 하지만, 의무기록에 동반 음독약물들의 용량까지 기록되어 있지 않아, 환자들의 acetaminophen 흡수와 대사에 미친 영향을 정량화 할 수 없는 한계가 존재한다.
- 음독 15시간 후 APAP 혈중농도가 검출된 35명 중 2명이 첫 번째 혈중농도 검사에서 100-치료선 아래의 비독성 농도를 보였으나, 후에 급성 간 손상을 보였다. 또 이 그룹 중 16명이 첫 번째 혈중농도 검사에서 100-치료선 위의 독성 농도를 보였고, 이 중 3명의 환자가, NAC 길항제 치료에도 불구하고 급성 간 독성을 보였다. 이는 첫 번째 혈중농도 검사를 통해 NAC 길항제 치료가 필요한 환자를 선별하는 것도 중요하지만, 최초 길항제 치료가 끝난 후 추가 치료가 필요한 환자를 선별하는 것도 매우 중요하다는 것을 보여준다.
- 음독 15시간 후 APAP 혈중농도 검출 예측을 위한 음독 후 내원까지 소요시간의 AUC와 절단값은 0.658, 450분으로, 높은 특이도로(85.6%) 약 8시간의 내원까지 소요시간을 절단값으로 계산했다. 2004년 미국 Food and Drug Administration은 APAP 급성 중독환자의 NAC 길항제 정주 치료를 음독 후 8–10시간 이내 시작할 것을 권고했고, 이 시간 이후 내원한 환자는 간 독성 발생의 위험이 높은 ‘late presenter’로 간주해왔다. 따라서 본 연구의 절단값, 음독 후 8시간은 그동안 다른 연구자들의 연구결과 그리고 그동안의 치료 권고와 다르지 않다2,4,6,12,13).
- 음독 후 늦게 내원한 환자들에게서 음독 15시간후 APAP 혈중농도가 더 높은 빈도로 검출되었다. 음독 후 상대적으로 일찍 내원한 환자들은, NAC 길항제 치료 종료 시 검사를 포함하여, APAP 혈중농도 검사를 더 많이 시행하게 되고, 음독 후 15시간 경과시각과 마지막 혈중농도 검사시각의 차이가 클 수 있다. 상관관계 분석을 시행하였고, 음독 후 병원에 오기까지 소요된 시간과 음독 후 15시간 경과시각과 마지막 APAP 혈중농도 검사시각과의 차이는 통계적으로 상관관계가 없었다(Spearman’s rho=0.106, p=0.157).
- 이 연구는 단일 국가 내 동아시아인으로 구성된 환자군의 자료를 기반으로 수행되었다. 동아시아인은 백인보다 APAP 흡수가 더 빠르고, 간 손상에 덜 취약한 것으로 알려져 있다. 따라서 첫 번째 혈중농도가 더 높게 나오고, 두 번째 혈중농도 검사에서 독성 농도가 검출되는(line-crossing) 빈도가 더 낮게 나왔을 가능성이 있다14-16).
- 본 연구는 후향적 관찰연구로, 환자 정보가 누락되거나 의무기록이 불완전한 경우, 선택 편향 및 데이터 입력오류가 있을 수 있다. 본 연구의 표본크기가 작아(n=181), 통계결과의 CI의 범위가 넓고, 비정규분포를 보여 연구결과의 일반화에 제약이 있을 수 있다. 연구대상 환자들의 단위체중당 음독용량이 상대적으로 낮은 편이서(중앙값 150.9 mg/kg), 다른 연구자들의 분석결과에 비해 100-치료선 이상의 APAP 독성 농도 검출빈도와 15시간 후 APAP 혈중농도 검출빈도가 상대적으로 낮을 수 있다.
고찰
- APAP 혈중농도를 치료 중 알 수 없는 환경에서, 14세 이상, 음독 후 15시간 이내 응급의료센터에 내원한 APAP 급성 중독환자를 영국 지침에 따라 치료할 때, 135 mg/kg 이상의 용량을 음독한 환자는 즉시 NAC 길항제 치료를 시작하고, 음독 후 8시간 이후에 내원한 환자는 정주 NAC 추가용량 투여를 고려하는 것이 안전하겠다.
결론
-
이해상충
이 연구에 영향을 미칠 수 있는 기관이나 이해당사자로부터 재정적, 인적 지원을 포함한 일체의 지원을 받은 바 없으며, 연구윤리와 관련된 제반 이해상충이 없음을 선언한다. 이 논문은 대한임상독성학회지와 다른 학회지에 동시 투고되지 않았으며 이전에 다른 학회지에 게재된 적이 없다.
Notes
-
Acknowledgement
- 본 연구를 위한 독성 데이터 수집에 헌신적인 노력을 해 준 성빈센트병원 응급의료센터 조은수 선생님께 본 지면을 빌어 깊은 감사를 전한다.
Fig. 1.The process of determining the research subjects; patients ≥14 years with acute acetaminophen poisoning presenting to emergency medical centers.
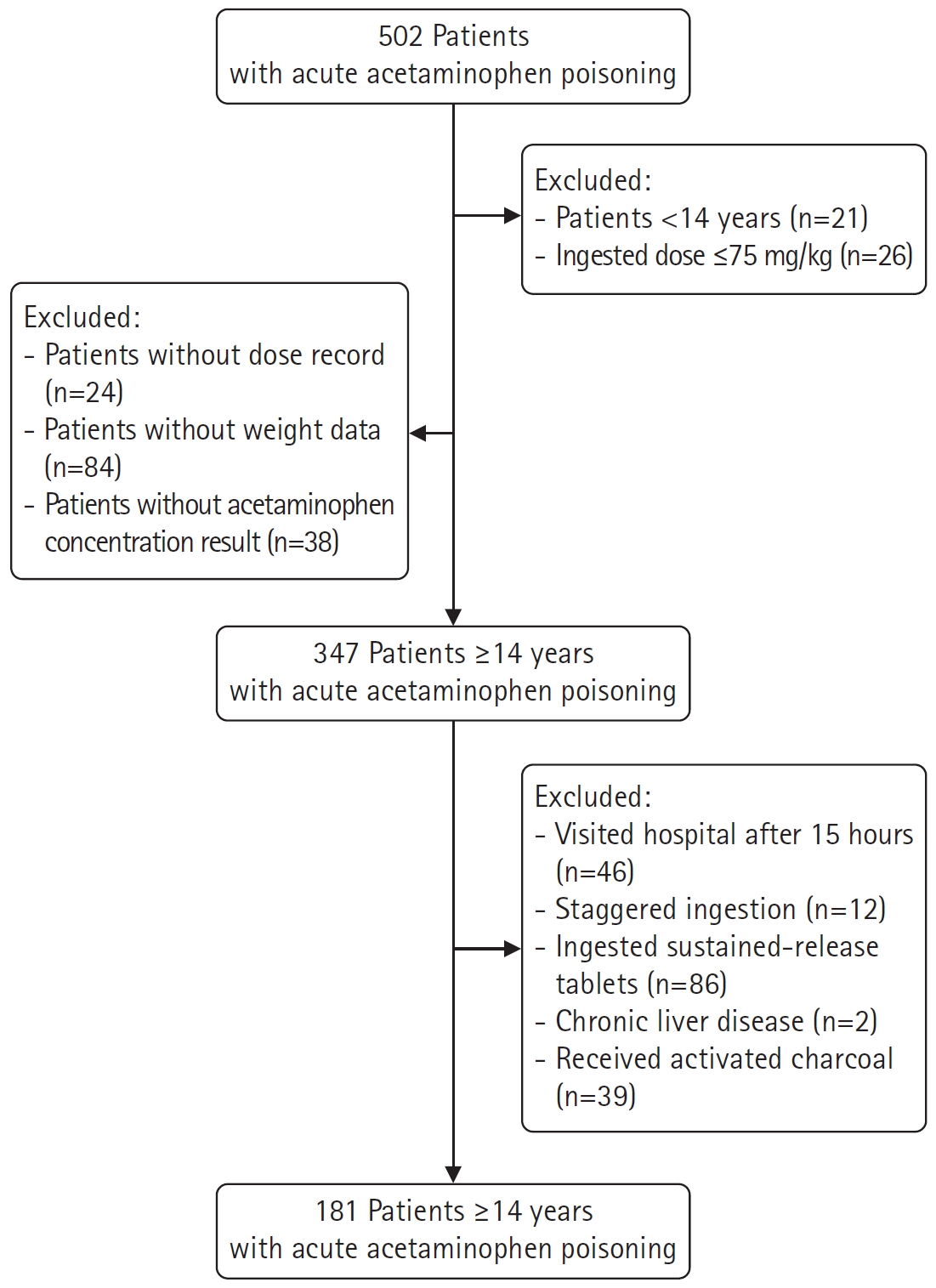

Fig. 2.The receiver operating characteristic curve of the ingested dose per unit weight for predicting the toxic concentration above the 100-line.
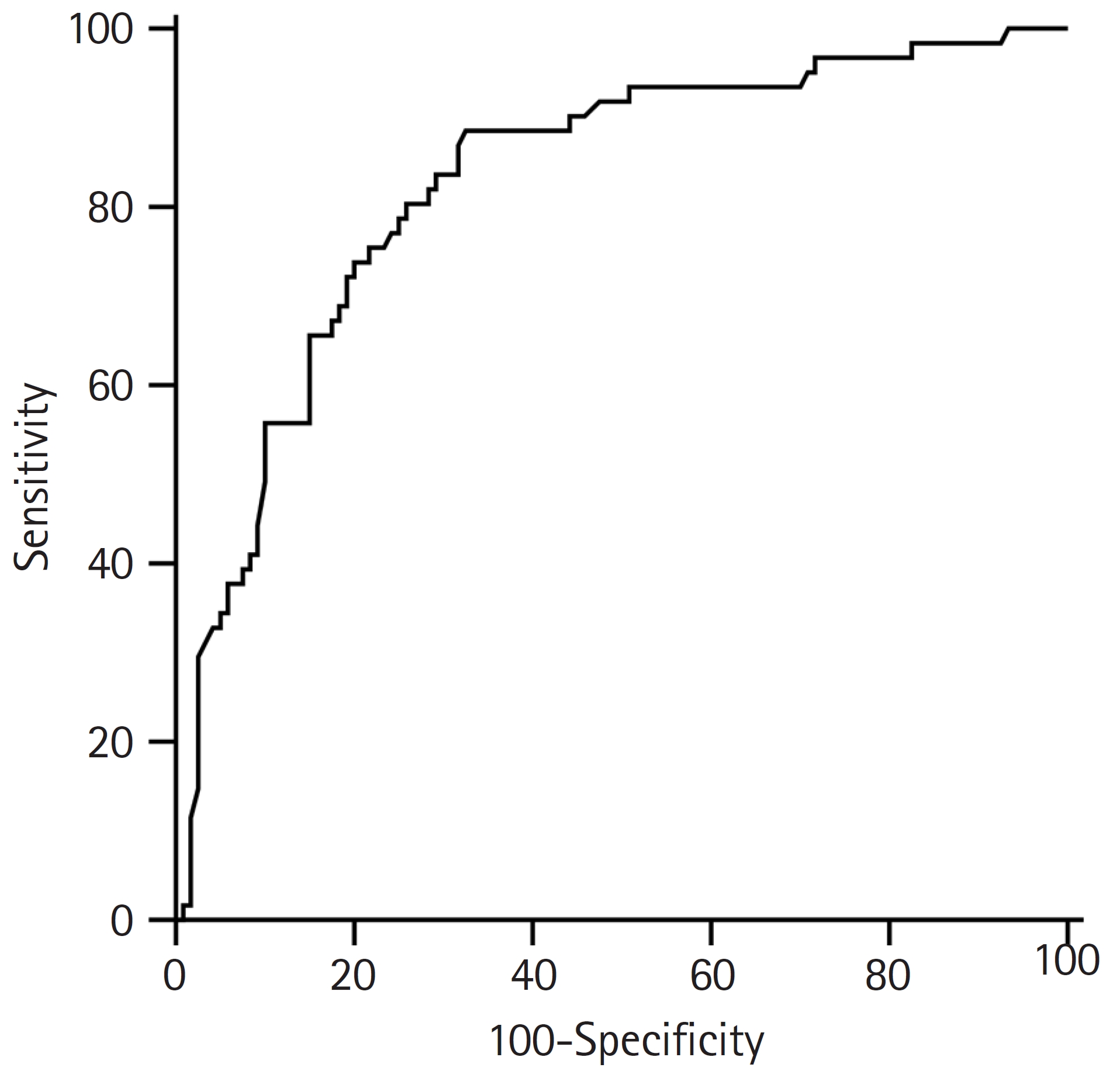

Fig. 3.Comparison of receiver operating characteristic curve of the ingested dose per unit weight, the time to visit the hospital and the combined prediction model for predicting acetaminophen detection after 15 hours.
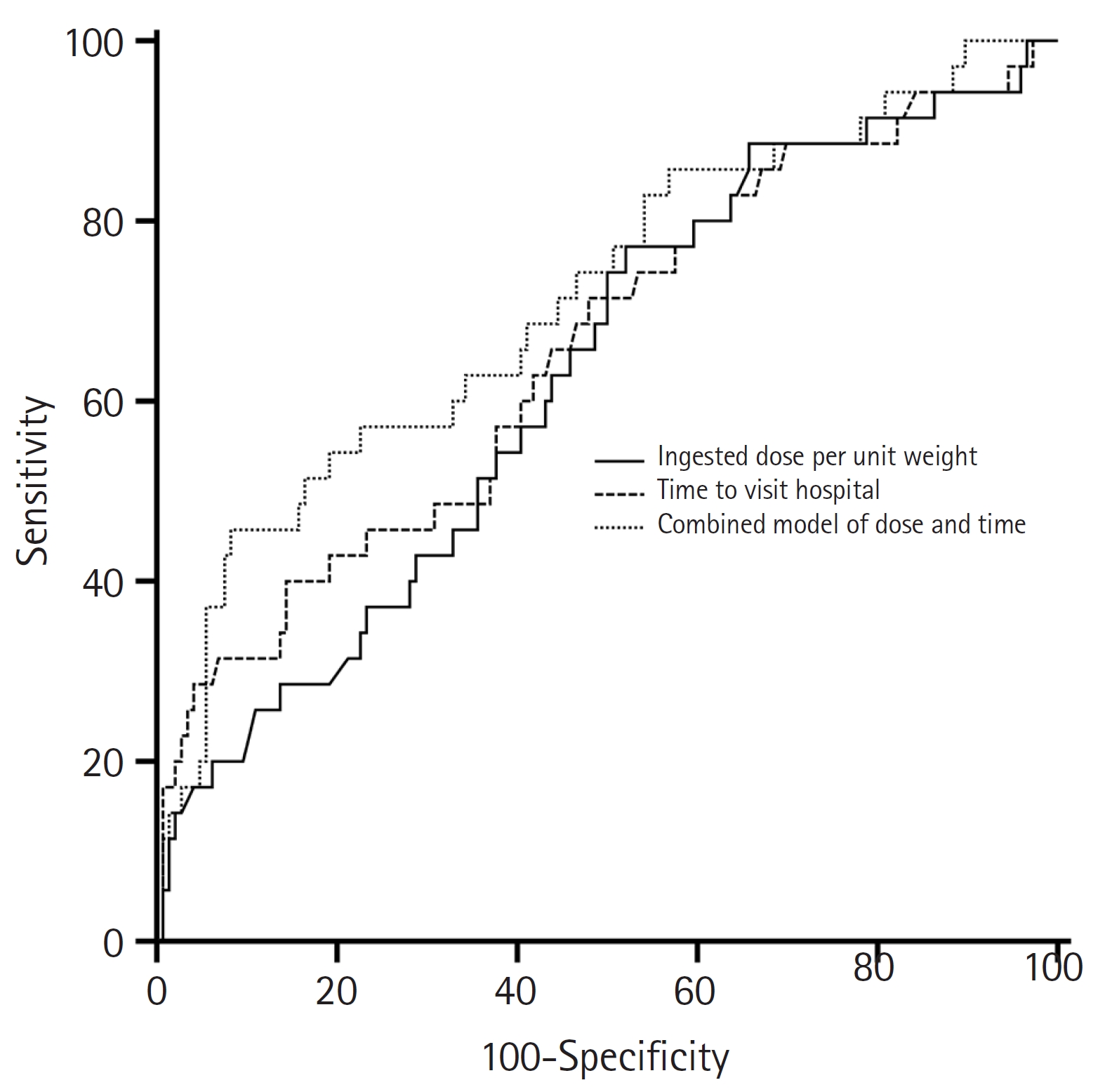

Table 1.Demographic and clinical characteristics of patients based on serum acetaminophen detection 15 hours after poisoning
Table 2.Logistic regression analysis for the detection of serum acetaminophen 15 hours after poisoning
Table 3.Comparison of area under the curve between clinical risk factors and combined prediction model for the detection of acetaminophen 15 hours after poisoning
- 1. Rumack BH, Matthew H. Acetaminophen poisoning and toxicity. Pediatrics 1975;55:871-6. https://doi.org/10.1542/peds.55.6.871ArticlePubMed
- 2. Rumack BH. Acetaminophen hepatotoxicity: the first 35 years. J Toxicol Clin Toxicol 2002;40:3-20. https://doi.org/10.1081/clt-120002882ArticlePubMed
- 3. Medicine and Healthcare Products Regulatory Agency, The Commission on Human Medicines. Paracetamol overdose: simplification of the use of intravenous acetylcysteine [Internet]. London: Medicine and Healthcare Products Regulatory Agency; 2012 [cited 2023 Sep 20]. Available from: https://webarchive.nationalarchives.gov.uk/20150110162216/http://www.mhra.gov.uk/Safetyinformation/Safetywarningsalertsandrecalls/Safetywarningsandmessagesformedicines/CON178225
- 4. Rumack BH, Bateman DN. Acetaminophen and acetylcysteine dose and duration: past, present and future. Clin Toxicol (Phila) 2012;50:91-8. https://doi.org/10.3109/15563650.2012.659252ArticlePubMed
- 5. Koppen A, van Riel A, de Vries I, Meulenbelt J. Recommendations for the paracetamol treatment nomogram and side effects of N-acetylcysteine. Neth J Med 2014;72:251-7.PubMed
- 6. Bateman DN, Dear JW. Acetylcysteine in paracetamol poisoning: a perspective of 45 years of use. Toxicol Res (Camb) 2019;8:489-98. https://doi.org/10.1039/c9tx00002jArticlePubMedPMC
- 7. Senarathna SM, Sri Ranganathan S, Buckley N, Fernandopulle R. A cost effectiveness analysis of the preferred antidotes for acute paracetamol poisoning patients in Sri Lanka. BMC Clin Pharmacol 2012;12:6. https://doi.org/10.1186/1472-6904-12-6ArticlePubMedPMC
- 8. Duffull SB, Isbister GK. Predicting the requirement for N-acetylcysteine in paracetamol poisoning from reported dose. Clin Toxicol (Phila) 2013;51:772-6. https://doi.org/10.3109/15563650.2013.830733ArticlePubMedPMC
- 9. Jeong HH, Cha K, Choi KH, So BH. Evaluation of cut-off values in acute paracetamol overdose following the United Kingdom guidelines. BMC Pharmacol Toxicol 2022;23:5. https://doi.org/10.1186/s40360-021-00547-1ArticlePubMedPMC
- 10. University Hospital of Leicester NHS Trust. Paracetamol poisoning: performa to guide ED management of oral ingestion in adults [Internet]. Leicester: University Hospital of Leicester NHS Trust; 2023 [cited 2023 Oct 7]. Available from: https://secure.library.leicestershospitals.nhs.uk/PAGL/Shared%20Documents/Paracetamol%20Overdose%20UHL%20Emergency%20Department%20Guideline.pdf
- 11. University Hospital of Leicester NHS Trust. Paracetamol poisoning in adults and children [Internet]. Leicester: University Hospital of Leicester NHS Trust; 2023 [cited 2023 Oct 7]. Available from: https://secure.library.leicestershospitals.nhs.uk/PAGL/Shared%20Documents/Paracetamol%20Overdose%20UHL%20Guideline.pdf
- 12. Department of Health and Human Services, Food and Drug Administration. The new drug application for the use of Acetadote (acetylcysteine) injection [Internet]. Silver Spring (MD): Food and Drug Administration; 2004 [cited 2023 Sep 20]. Available from: https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2004/21539ltr.pdf
- 13. Department of Health and Human Service, Food and Drug Administration. Intravenous N-acetylcysteine [Internet]. Silver Spring (MD): Food and Drug Administration; 2004 [cited 2023 Sep 20]. Available from: https://www.accessdata.fda.gov/drugsatfda_docs/label/2004/21539_N-acetylcysteine_lbl.pdf
- 14. Critchley JA, Nimmo GR, Gregson CA, Woolhouse NM, Prescott LF. Inter-subject and ethnic differences in paracetamol metabolism. Br J Clin Pharmacol 1986;22:649-57. https://doi.org/10.1111/j.1365-2125.1986.tb02953.xArticlePubMedPMC
- 15. Lee HS, Ti TY, Koh YK, Prescott LF. Paracetamol elimination in Chinese and Indians in Singapore. Eur J Clin Pharmacol 1992;43:81-4. https://doi.org/10.1007/BF02280759ArticlePubMed
- 16. Critchley JA, Critchley LA, Anderson PJ, Tomlinson B. Differences in the single-oral-dose pharmacokinetics and urinary excretion of paracetamol and its conjugates between Hong Kong Chinese and Caucasian subjects. J Clin Pharm Ther 2005;30:179-84. https://doi.org/10.1111/j.1365-2710.2004.00626.xArticlePubMed
References
Figure & Data
References
Citations
Citations to this article as recorded by 


 KSCT
KSCT
 PubReader
PubReader ePub Link
ePub Link Cite
Cite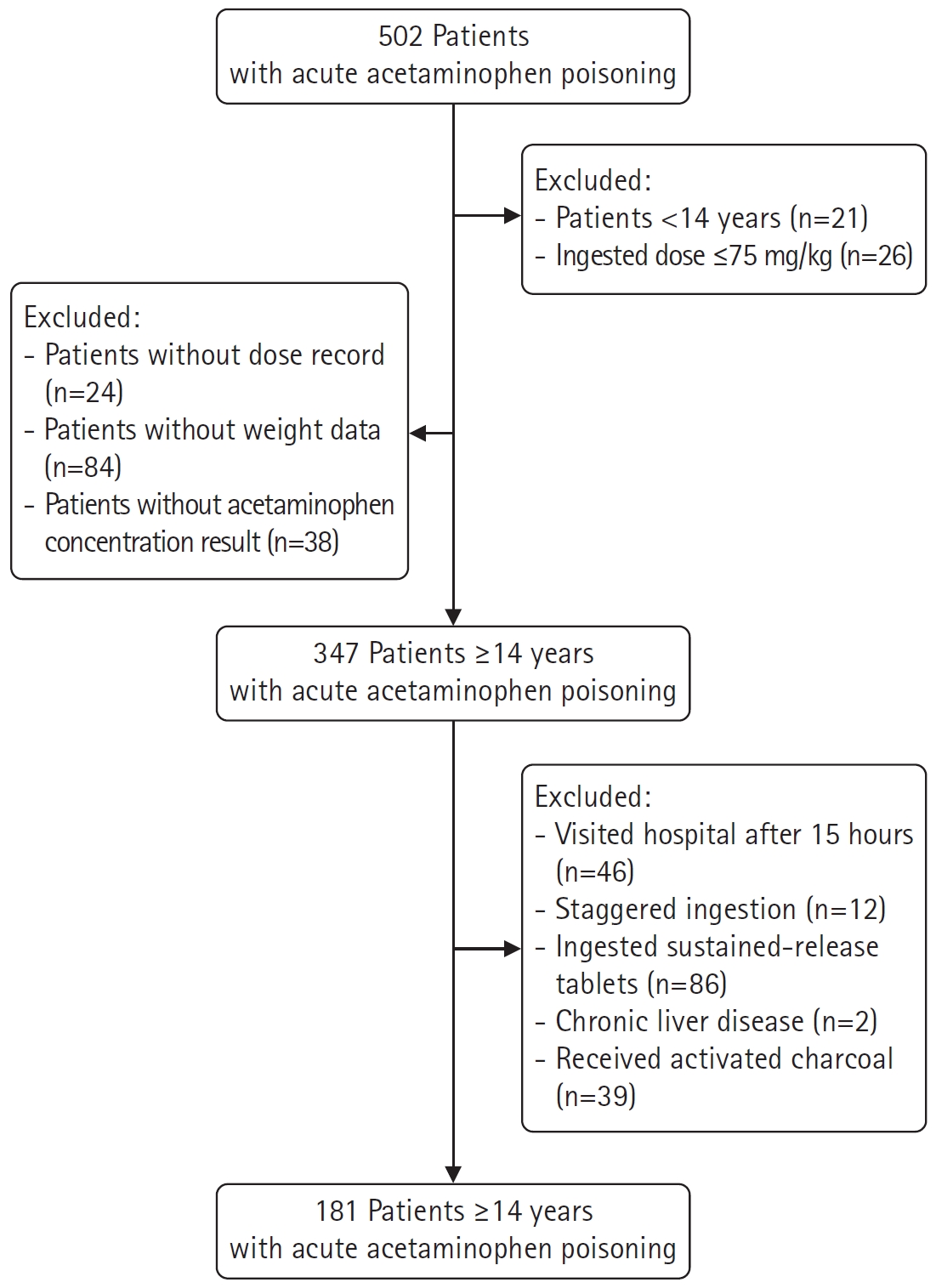




 Korean Society of Clinical Toxicology
Korean Society of Clinical Toxicology